https://ria.ru/20210309/vaktsina-1600497813.html
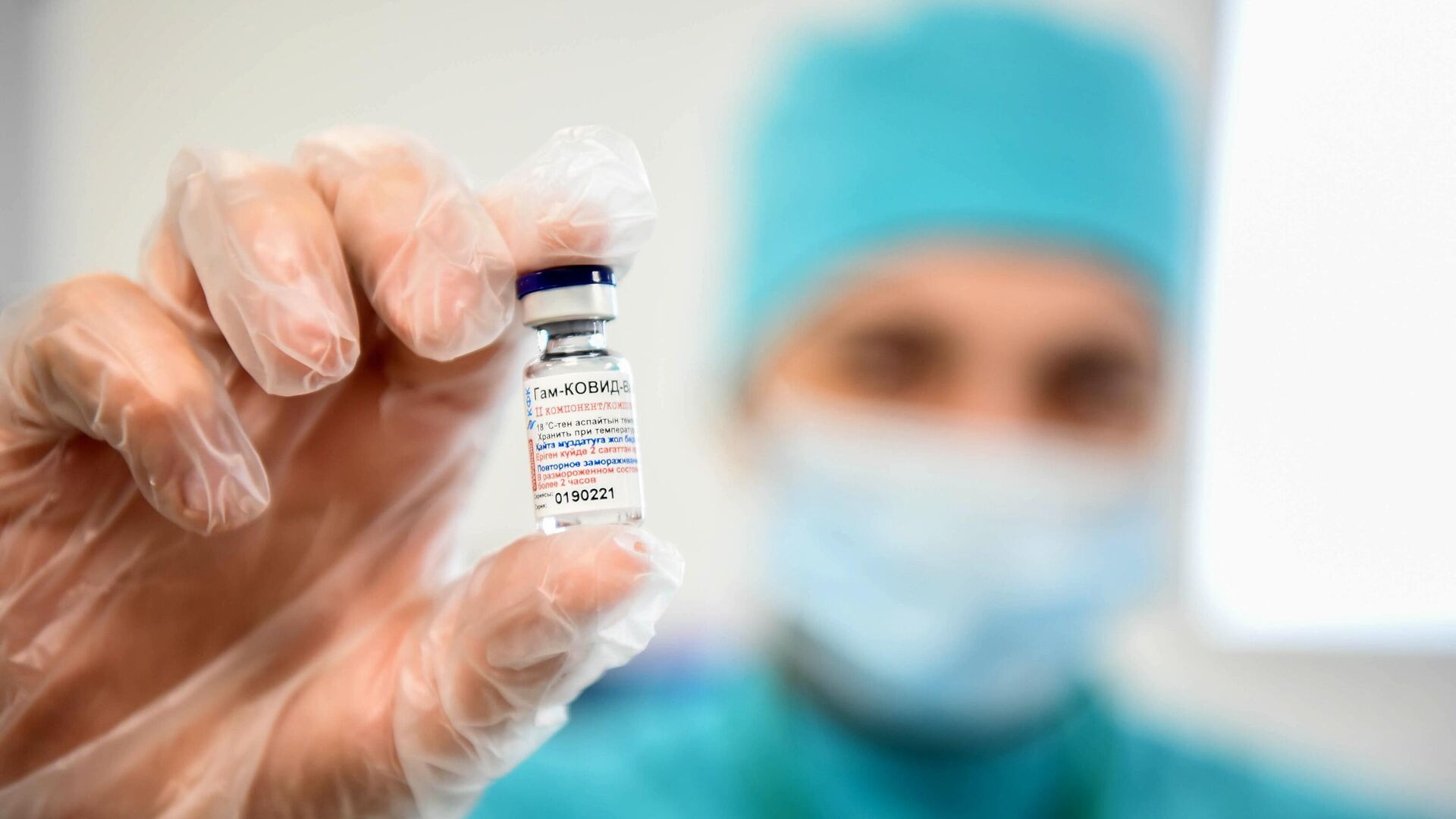
Регулятор ЕС изучит соответствие "Спутника V" стандартам Евросоюза
Регулятор ЕС изучит соответствие "Спутника V" стандартам Евросоюза - РИА Новости, 09.03.2021
Регулятор ЕС изучит соответствие "Спутника V" стандартам Евросоюза
Европейский лекарственный регулятор ЕМА при проведении оценки российской вакцины против коронавируса "Спутник V" проверит ее соответствие обычным стандартам... РИА Новости, 09.03.2021
2021-03-09T17:17
2021-03-09T17:17
2021-03-09T17:47
распространение коронавируса
в мире
евросоюз
коронавирус covid-19
вакцина "спутник v"
https://cdnn21.img.ria.ru/images/07e5/03/03/1599761128_0:160:3072:1888_1920x0_80_0_0_b64629ed4c377cbf4884bbc43530c524.jpg
БРЮССЕЛЬ, 9 мар – РИА Новости. Европейский лекарственный регулятор ЕМА при проведении оценки российской вакцины против коронавируса "Спутник V" проверит ее соответствие обычным стандартам Евросоюза, любое решение ЕМА по вакцине будет основано исключительно на научных данных о ее эффективности и безопасности, сообщил РИА Новости во вторник представитель европейского регулятора."ЕМА в настоящее время оценивает вакцину против COVID-19 "Спутник V" по процедуре постепенной экспертизы rolling review. ЕМА оценит соответствие "Спутник V" обычным стандартам ЕС, любая рекомендация будет базироваться на научных данных, подтверждающих безопасность, качество и эффективность вакцины, и ни на чем ином", - подчеркнул собеседник агентства.Он добавил, что ЕМА "будет изучать данные по мере их поступления, чтобы решить, превышают ли преимущества вакцины связанные с ней риски. "Постепенная экспертиза будет продолжаться до тех пор, пока не соберется достаточно доказательств для подачи формальной заявки на авторизацию", - отметил представитель европейского регулятора.Отвечая на просьбу РИА Новости прокомментировать слова одного из руководителей EMA и представителя австрийского национального лекарственного регулятора Кристы Виртумер-Хохе, которая на днях сравнила перспективу экстренного одобрения "Спутник V" в Австрии с "игрой в русскую рулетку", собеседник агентства отметил, что ЕС всегда выступал за централизованное одобрение вакцин против коронавируса, такая общеевропейская позиция, по его словам, была выработана в ноябре прошлого года, еще до одобрения в Евросоюзе первой антикоронавирусной вакцины."Позиция европейской регулирующей сети в отношении национальных разрешений для вакцин изложена в заявлении от 20 ноября 2020 года. Это позиция национальных компетентных органов и ЕМА была обозначена еще в самом начале, до того, как какая-либо вакцина была одобрена, и эта позиция не нова", - указал представитель ЕМА.Он сослался на заявление от 20 ноября прошлого года. Тогда в ЕМА напомнили, что вакцины против коронавируса, при производстве которых задействованы сложные биохимические процессы, попадают под положение ЕС 726 от 2004 года. Это положение, в частности, предусматривает централизованную процедуру одобрения таких лекарственных препаратов европейским регулятором ЕМА.Кроме того, в заявлении указывается, что ЕМА, совместно с главами национальных агентств по лекарственным препаратам Евросоюза, призывают производителей вакцин подавать заявки на одобрение препаратов в ЕС именно через централизованную процедуру. Такая процедура, согласно заявлению, должна гарантировать "справедливый доступ к вакцине всех членов Евросоюза в одно и то же время при обеспечении эффективного контроля препарата на всех этапах".Российская вакцина против коронавируса "Спутник V" с 4 марта проходит процедуру постепенной экспертизы в Европейском агентстве по лекарственным средствам ЕМА, которое занимается одобрением вакцин для использования на европейском рынке. Ранее в ЕМА выразили надежду, что оценка "Спутник V" пройдет в ускоренные сроки, но даты одобрения вакцины пока нет.В настоящее время на рынке Евросоюза авторизованы три вакцины: компаний Pfizer/BioNTech (закупка до 600 миллионов доз), Moderna (два контракта до 460 миллионов доз) и AstraZeneca (до 400 миллионов доз).Кроме того, ЕК заключила контракты на поставки в ЕС вакцин с компаниями Johnson&Johnson, Sanofi-GSK, CureVac. До настоящего момента Sanofi-GSK и CureVac еще не подали заявки для авторизации своих препаратов на рынке ЕС, J&J подала заявку 16 февраля, ее одобрение ожидается 11 марта. CureVac 12 февраля сделала запрос на проведение процедуры постепенной экспертизы rolling review.Всего страны ЕС благодаря контрактам Еврокомиссии смогут получить доступ более чем к 2,3 миллиарда доз антикоронавирусных вакцин. В ЕС ожидают, что к середине сентября в Европе уже будут привиты порядка 70% жителей.В последние недели ЕС столкнулся с рядом проблем в поставках одобренных для использования в союзе вакцин, в частности, компаний Pfizer/BioNTech и AstraZeneca. Задержки в поставках могут сорвать амбициозные планы Брюсселя по вакцинации.Применение вакцины "Спутник V" одобрено уже более чем в 40 странах мира.
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2021
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
распространение коронавируса, в мире, евросоюз, коронавирус covid-19, вакцина "спутник v"
Распространение коронавируса, В мире, Евросоюз, Коронавирус COVID-19, Вакцина "Спутник V"
БРЮССЕЛЬ, 9 мар – РИА Новости. Европейский лекарственный регулятор ЕМА при проведении оценки российской вакцины против коронавируса "Спутник V" проверит ее соответствие обычным стандартам
Евросоюза, любое решение ЕМА по вакцине будет основано исключительно на научных данных о ее эффективности и безопасности, сообщил РИА Новости во вторник представитель европейского регулятора.
"ЕМА в настоящее время оценивает вакцину против COVID-19 "Спутник V" по процедуре постепенной экспертизы rolling review. ЕМА оценит соответствие "Спутник V" обычным стандартам ЕС, любая рекомендация будет базироваться на научных данных, подтверждающих безопасность, качество и эффективность вакцины, и ни на чем ином", - подчеркнул собеседник агентства.
Он добавил, что ЕМА "будет изучать данные по мере их поступления, чтобы решить, превышают ли преимущества вакцины связанные с ней риски. "Постепенная экспертиза будет продолжаться до тех пор, пока не соберется достаточно доказательств для подачи формальной заявки на авторизацию", - отметил представитель европейского регулятора.
Отвечая на просьбу РИА Новости прокомментировать слова одного из руководителей EMA и представителя австрийского национального лекарственного регулятора Кристы Виртумер-Хохе, которая на днях сравнила перспективу экстренного одобрения "Спутник V" в
Австрии с "игрой в русскую рулетку", собеседник агентства отметил, что ЕС всегда выступал за централизованное одобрение вакцин против коронавируса, такая общеевропейская позиция, по его словам, была выработана в ноябре прошлого года, еще до одобрения в Евросоюзе первой антикоронавирусной вакцины.
"Позиция европейской регулирующей сети в отношении национальных разрешений для вакцин изложена в заявлении от 20 ноября 2020 года. Это позиция национальных компетентных органов и ЕМА была обозначена еще в самом начале, до того, как какая-либо вакцина была одобрена, и эта позиция не нова", - указал представитель ЕМА.
Он сослался на заявление от 20 ноября прошлого года. Тогда в ЕМА напомнили, что вакцины против коронавируса, при производстве которых задействованы сложные биохимические процессы, попадают под положение ЕС 726 от 2004 года. Это положение, в частности, предусматривает централизованную процедуру одобрения таких лекарственных препаратов европейским регулятором ЕМА.
Кроме того, в заявлении указывается, что ЕМА, совместно с главами национальных агентств по лекарственным препаратам Евросоюза, призывают производителей вакцин подавать заявки на одобрение препаратов в ЕС именно через централизованную процедуру. Такая процедура, согласно заявлению, должна гарантировать "справедливый доступ к вакцине всех членов Евросоюза в одно и то же время при обеспечении эффективного контроля препарата на всех этапах".
Российская вакцина против коронавируса "Спутник V" с 4 марта проходит процедуру постепенной экспертизы в Европейском агентстве по лекарственным средствам ЕМА, которое занимается одобрением вакцин для использования на европейском рынке. Ранее в ЕМА выразили надежду, что оценка "Спутник V" пройдет в ускоренные сроки, но даты одобрения вакцины пока нет.
В настоящее время на рынке Евросоюза авторизованы три вакцины: компаний Pfizer/BioNTech (закупка до 600 миллионов доз), Moderna (два контракта до 460 миллионов доз) и
AstraZeneca (до 400 миллионов доз).
Кроме того, ЕК заключила контракты на поставки в ЕС вакцин с компаниями
Johnson&Johnson, Sanofi-GSK, CureVac. До настоящего момента Sanofi-GSK и CureVac еще не подали заявки для авторизации своих препаратов на рынке ЕС, J&J подала заявку 16 февраля, ее одобрение ожидается 11 марта. CureVac 12 февраля сделала запрос на проведение процедуры постепенной экспертизы rolling review.
Всего страны ЕС благодаря контрактам
Еврокомиссии смогут получить доступ более чем к 2,3 миллиарда доз антикоронавирусных вакцин. В ЕС ожидают, что к середине сентября в
Европе уже будут привиты порядка 70% жителей.
В последние недели ЕС столкнулся с рядом проблем в поставках одобренных для использования в союзе вакцин, в частности, компаний Pfizer/BioNTech и AstraZeneca. Задержки в поставках могут сорвать амбициозные планы
Брюсселя по вакцинации.
Применение вакцины "Спутник V" одобрено уже более чем в 40 странах мира.