МОСКВА, 4 окт — РИА Новости. Специалисты Национального исследовательского ядерного университета "МИФИ", совместно с исследователями университета Нанта и Реймского университета Шампань-Арденн (Франция), разработали микрочип на основе квантовых точек, позволяющий выявлять эффективные ингибиторы (вещества, способные снижать активность) ферментов, которые восстанавливают ДНК раковых клеток в ответ на радиотерапию и воздействие противораковых препаратов — это позволит повысить эффективность онкотерапии во много раз. Результаты исследования опубликованы в журнале Scientific Reports.
Терапевтический эффект многих противораковых препаратов основан на их способности вызывать повреждения ДНК, в том числе двунитевые разрывы, которые "чинятся" (репарируются) специальными ферментами.
По словам ученых НИЯУ МИФИ, для создания новых ингибиторов ферментов необходима разработка высокопроизводительного инструментария, позволяющего выявить наиболее активные ингибиторы и оценить их эффективность.
"Мы разработали микрочип с квантовыми точками в качестве флуоресцентных меток для оценки изменений активности фермента "ДНК-зависимой протеинкиназы" (кратко — "киназы") в ответ на повреждение ДНК. Было показано, что использование квантовых точек в качестве меток позволяет отследить, как ингибиторы влияют на активность ферментов в ответ на повреждение ДНК", — говорит ведущий учёный международной лаборатории нано-биоинженерии НИЯУ МИФИ, профессор Реймского университета Игорь Набиев.
В настоящее время в качестве флуоресцентных меток в микрочипах обычно используются органические красители, которые зачастую оказываются малочувствительными и нестабильными из-за фотодеградации. Новые данные говорят о том, что перспективная альтернатива – квантовые точки, флуоресцентные полупроводниковые нанокристаллы.
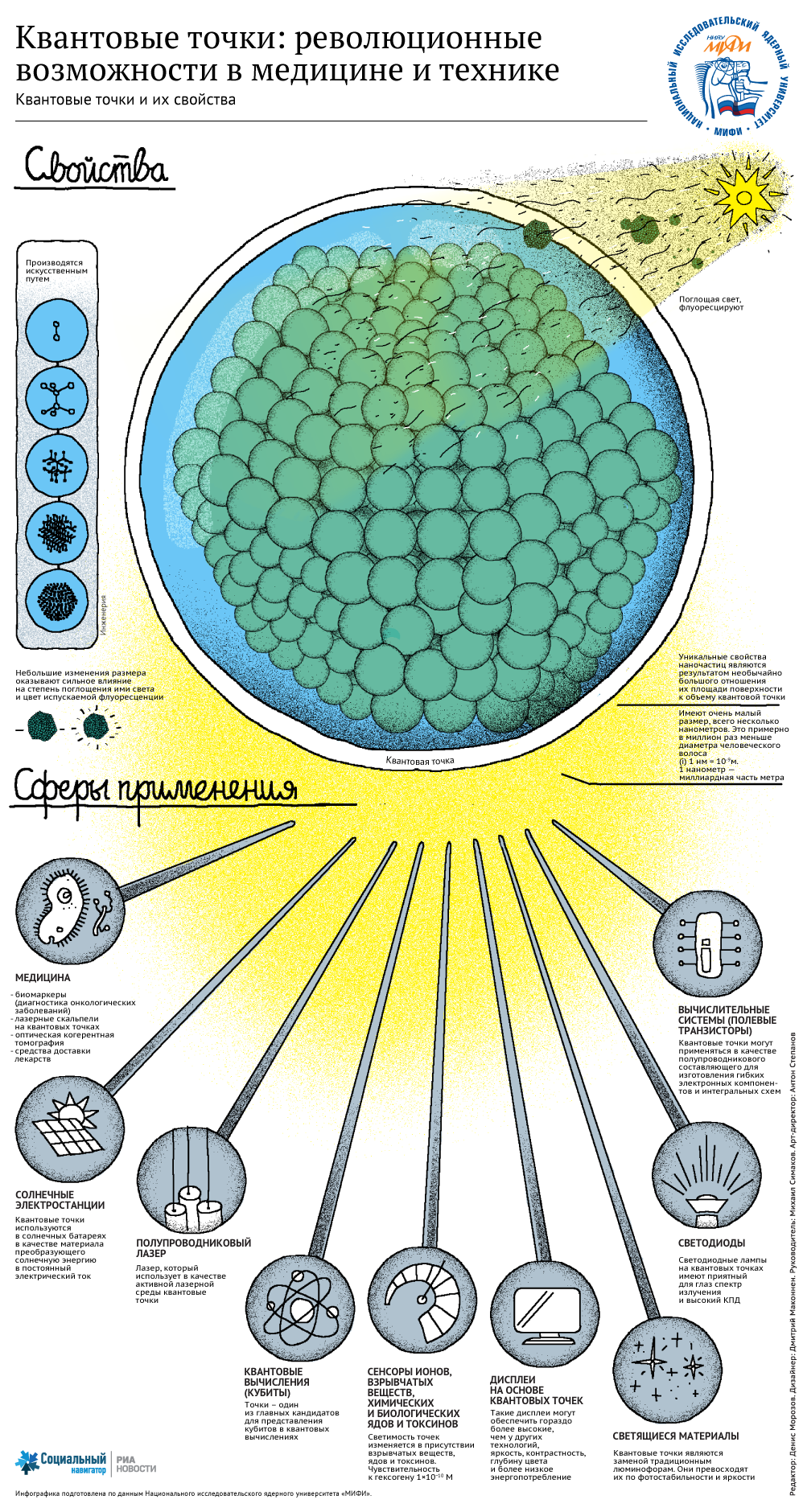
Оптические свойства квантовых точек уникальны: помимо высокой устойчивости к выцветанию, они способны поглотить огромное количество световой энергии и обладают рекордно яркой люминесценцией.
Киназа DNA-PKcs играет ключевую роль в формировании лекарственной и радио-резистентности опухоли, являясь важным звеном механизма репарации ДНК. Исследования на животных показали, что ингибирование DNA-PKcs низкомолекулярными ингибиторами приводит к радио- и хемосенсибилизации таких злокачественных опухолей, как остеосаркома, глиома, а также рак молочной железы, легкого и толстой кишки.
Ожидается, что разработка и скрининг ингибиторов DNA-PKcs киназ повысит эффективность существующих методов противораковой терапии, основанных на повреждении ДНК опухолевых клеток.
В опубликованной статье проводится оценка перспективности предлагаемой системы в качестве инструмента для скрининга ингибиторов киназы с целью повышения эффективности противораковой терапии.