МОСКВА, 8 мар — РИА Новости, Альфия Еникеева. Среди российских ученых — сорок процентов женщин. Есть научные коллективы, состоящие практически полностью из представительниц прекрасного пола. Один из них, базирующийся в Медико-генетическом научном центре (МГНЦ), готовит серьезный прорыв в лечении мусковисцидоза — тяжелого наследственного заболевания, пока неизлечимого.
Наука женского рода
"Я тут с парнем из лаборатории функциональной геномики разговаривала. Он три часа объяснял, что такое ген. А вот на вопрос, что такое любовь, ответил: чувство сильной привязанности", — улыбается научный сотрудник лаборатории редактирования генома МГНЦ Екатерина Кондратьева, рассматривая в чашках Петри клеточные культуры, выращиванием которых она занимается последние полгода.
Сотрудницы заняты повседневными делами. Одни загружают в центрифугу пробирки с молекулами ДНК, кто-то проверяет результаты полимеразной цепной реакции или запускает процесс превращения обычных соматических клеток человека в стволовые.
Лабораторию редактирования генома МГНЦ с полным правом можно назвать женским царством. Здесь под руководством российского генетика Светланы Смирнихиной девять молодых исследовательниц решают амбициозные задачи. В ближайшие несколько лет они намерены победить мусковисцидоз и тяжелое наследственное заболевание глаз — так называемую плоскую роговицу.

© Иллюстрация РИА Новости . Источник: Расчеты Института статистических исследований и экономики знаний НИУ ВШЭ, основанных на данных Росстата
Доля женщин среди российских ученых
Разрезать и правильно склеить
"Вы не подумайте, мужчины у нас тоже работают. Просто их не так много", — объясняет Светлана Смирнихина, провожая меня в соседнюю с лабораторией комнату. Здесь только компьютеры и кипы листов со схемами генетических конструкций.
Именно в этом кабинете начинаются все исследовательские проекты лаборатории. Прежде чем приступить к редактированию генома, ученые в компьютерной программе создают различные варианты плазмид — небольших молекул ДНК, физически отдельных от хромосом и способных самостоятельно воспроизводить самих себя.
Такие плазмиды со вставленными в них дополнительными генами ферментов — необходимые компоненты геномного редактора CRISPR/Cas9. Система также включает в себя молекулу РНК, в которую можно добавить желаемый участок узнавания в геноме и участок взаимодействия с белком-ферментом Cas9. Именно он разрезает ДНК в том месте, которое надо исправить.
"Когда возникает разрыв, клетка его пытается сшить. Если мы даем клетке правильную молекулу ДНК, она может встроить ее вместо этого разрыва. И таким образом мы исправим мутацию. В нашей работе по мусковисцидозу такая молекула — вот эта плазмида", — исследовательница показывает на правую нижнюю молекулу на цветной схеме.

© ФГБНУ "Медико-генетический научный центр"
Слева чашки Петри, в которых наращиваются плазмиды в бактериях. Справа схемы (карты) плазмид для редактирования
Выбор конструкции был настолько удачен, что генетики даже не решаются называть точный процент клеток, в которых мутацию удалось исправить. Говорят, что все перепроверят, но если данные подтвердятся сначала на культурах клеток, а потом на модельных животных, то в перспективе можно будет вести речь об излечении от некоторых форм мусковисцидоза — тяжелого наследственного заболевания, при котором страдают легкие и поджелудочная железа. Правда, при условии, что их методику разрешат применять с самого рождения. Если же с шести лет — полностью победить болезнь не получится, но продолжительность жизни пациентов увеличится.
"Мы исправляем самую распространенную в мире мутацию в гене CFTR, вызывающую мусковисцидоз. Взяли клетки кожи пациента, страдающего этим заболеванием, и перепрограммировали их в стволовые. Затем вставили в них выращенные в лабораторных условиях плазмиды. Последний, пятый вариант оказался самым удачным. Это послужило инструментом для того, чтобы восстановить правильную цепь ДНК. В результате мутация исправилась более чем в десяти процентах клеток. Более точную цифру называть не хочу. Самим пока не верится, потому что это — очень хороший результат. Ни у кого в мире еще не получалось выйти за рамки пяти процентов", — уточняет Светлана Смирнихина.
Можно без ножниц
Сотрудницы лаборатории редактирования генома одними из первых в России использовали систему CRISPR/Cas9. Сегодня они испытывают новые варианты этого редактора, которые позволяют исправлять мутации, не разрезая нить ДНК. Известно, что именно разрыв ДНК приводит к нежелательным последствиям при редактировании человеческого генома: делециям — хромосомным перестройкам, когда теряется участок последовательности.
"При применении классического варианта CRISPR/Cas9 часто возникают не те изменения, которые мы хотим получить. Поэтому ученые придумали модификацию этой системы. В ней белок Cas9 не является каталитически активным, то есть он, как и раньше, может прийти в нужное место, но не способен разрезать ДНК. Он меняет один нуклеотид на другой, не трогая нить, благодаря тому, что соединен с ферментом цитидиндезаминазой", — рассказывает генетик Екатерина Кондратьева.

© ФГБНУ "Медико-генетический научный центр"
Классический и модифицированный варианты геномного редактора CRISPR/Cas9
Второй год она вместе с коллегами с помощью улучшенной технологии CRISPR/Cas9 пытается исправить мутацию в гене KERA, приводящую к возникновению плоской роговицы глаза.
"Мы уже модифицировали культуру человеческих клеток. Ввели в нее матрицу, содержащую мутацию, туда же добавили инструмент, который должен редактировать эту мутацию, и культивировали некоторое время. Буквально на днях мы эту матрицу извлекли и изучаем, исправились мутации или нет. Но это не очень быстрый процесс. У нас ведь только один нуклеотид должен был поменяться в процессе редактирования, а это трудно засечь. Поэтому сейчас мы работаем над методикой, которая позволит нам увидеть, состоялось редактирование или нет", — объясняет Кондратьева.
По словам Светланы Смирнихиной, даже при десятипроцентной эффективности редактирования можно говорить о возможности исправления плоской роговицы у людей.

Светлана Смирнихина рассматривает в чашке Петри культуру человеческих клеток
1 из 4
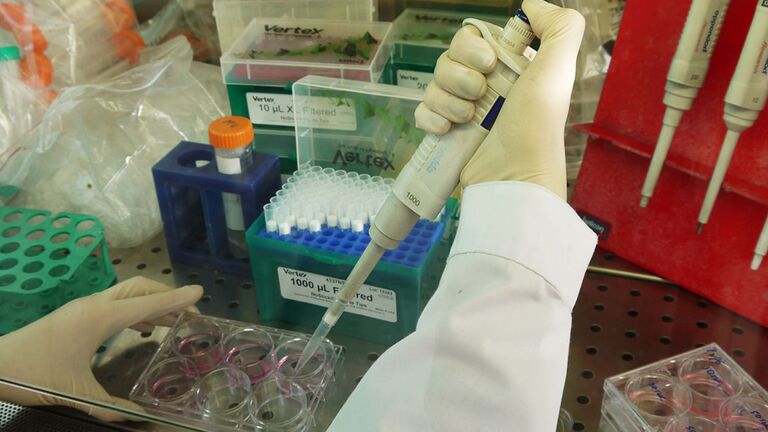

Сотрудница лаборатории редактирования генома анализирует результаты редактирования методом CRISPR-Cas9
3 из 4

Светлана Смирнихина рассматривает в чашке Петри культуру человеческих клеток
1 из 4
Сотрудница лаборатории редактирования генома анализирует результаты редактирования методом CRISPR-Cas9
3 из 4
"Если все получится, а исследования займут еще несколько лет, то будет два варианта лечения. Первый — взять у пациента клетки, репрограммировать их в стволовые, затем в них исправить мутацию и трансплантировать эти клетки больному. Второй — внутривенно ввести эту систему, и она сама найдет те клетки, которые нужно исправить, и исправит их. К сожалению, модифицированную технологию CRISPR/Cas9 нельзя использовать для всех генетических поломок, но около трех тысяч патогенных мутаций она отредактировать сможет. Вообще мы, кажется, первые в России применяем геномный редактор "без ножниц". Все о нем знают, но никто им не пользовался", — говорит биолог.
На вопрос, ощущают ли они себя первопроходцами, Екатерина Кондратьева и Светлана Смирнихина почти синхронно отвечают: "Ощущаем".
"Но без этого в науке нельзя", — улыбаясь, добавляет Смирнихина.